Chapitre 3 : Méthodes chimiques d’analyse⚓︎
▶️ Capsule : Le cours complet
▶️ Capsule : Le cours complet 2
I. 🔎 Principe du dosage par titrage (Rappels de première)⚓︎
A savoir
👉 Doser une espèce chimique dans une solution consiste à déterminer sa concentration (molaire ou massique) ou la quantité de matière dans un échantillon.
⚗️ Le dosage par titrage permet de déterminer la quantité de matière d’une espèce en exploitant une réaction chimique.

- L’espèce titrée réagit avec une espèce de concentration connue appelée titrant.
- On mesure la quantité précise d’espèce titrante nécessaire pour doser l’espèce titrée.
- Un dosage par titrage direct s’appuie sur une réaction chimique, appelée réaction support de titrage, qui doit être être rapide, totale et unique.
- Le volume de solution contenant l’espèce titrée est appelé prise d’essai.
➡️ À l’équivalence, les réactifs sont introduits dans les proportions stœchiométriques de la réaction : l y a alors changement de réactif limitant.
On réalise le titrage d’une solution A, de concentration inconnue \(C_A\) et de volume \(V_A\), par une solution B, de concentration connue \(C_B\) selon la réaction de titrage :
On note \(V_B\) le volume versé et \(V_{E}\) le volume de réactif titrant à l’équivalence.
À l’équivalence on a la relation suivante :
➡️ On en déduit la concentration \(C_A\).
💡 En 1ère, on a vu des titrages colorimétriques où l’équivalence est repérée par un changement de couleur du mélange réactionnel.
▶️ Capsule : Rappels sur les titrages colorimétriques
II. 📈 Méthodes de suivi d’un titrage⚓︎
A savoir
1. 🧪 Titrage pH-métrique⚓︎
▶️ Capsule : Titrage pH-métrique
Un titrage pH-métrique consiste à suivre l’évolution du pH de la solution titrée au cours de l’ajout de la solution titrante. La réaction support du titrage est une réaction acido-basique entre un couple titrant et un couple titré.
On mesure le pH de la solution titrée pour chaque volume de solution titrante versée en ajoutant la solution titrante mL par mL (ou tous les ½ mL autour de l’équivalence).
La courbe de titrage pH-métrique est la courbe \(pH = f(V_{Sol.titrante versée})\) donnant les variations du pH en fonction du volume de solution titrante versée.
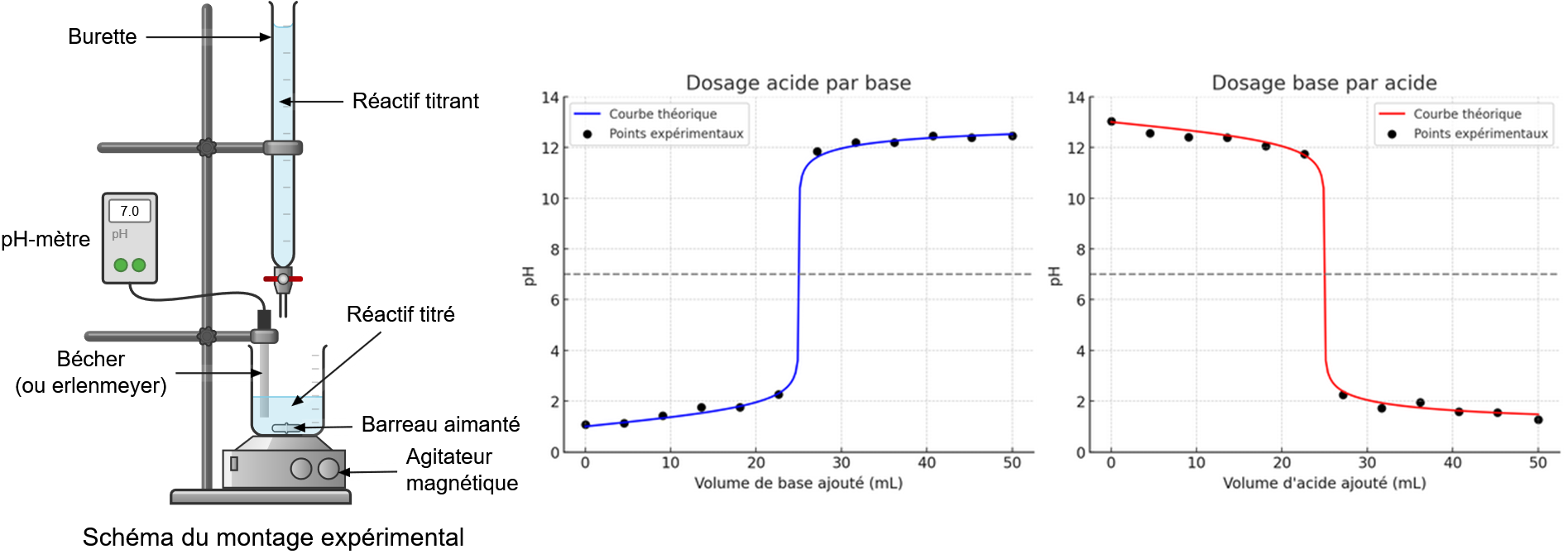
👉 L’équivalence est repérée expérimentalement lorsqu’il se produit une brusque variation du pH, appelée saut de pH.
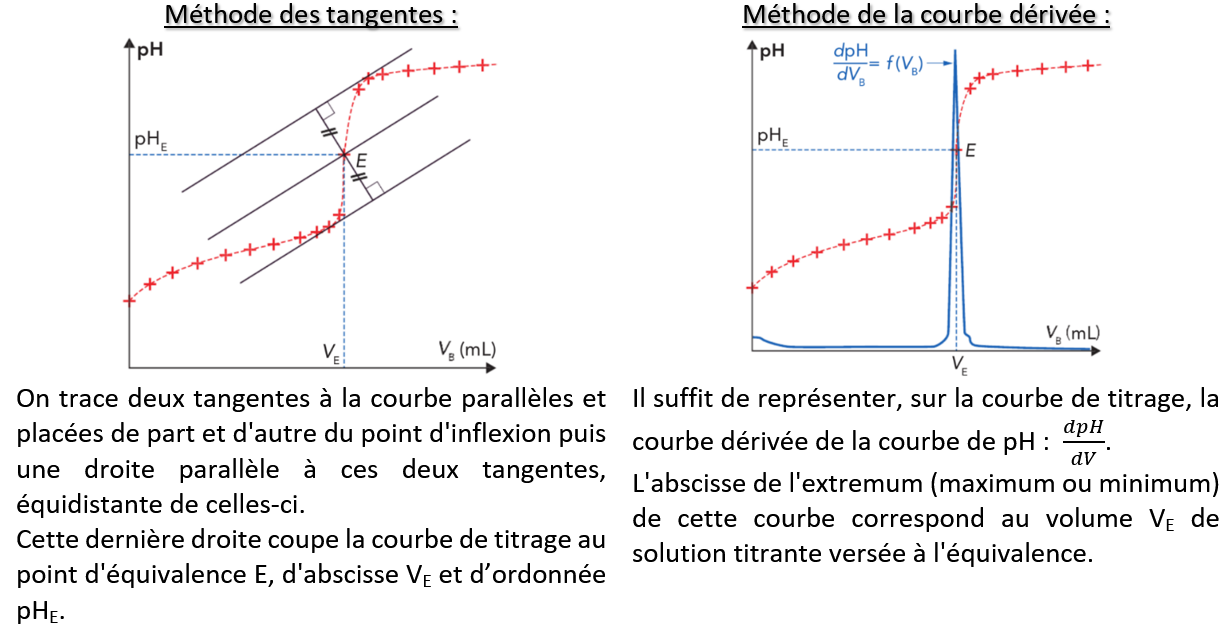
On peut déterminer expérimentalement les coordonnées du point d’équivalence sur la courbe de titrage par deux méthodes :
2. ⚡ Titrage conductimétrique⚓︎
a) Principe⚓︎
▶️ Capsule : Titrage conductimétrique
Un titrage conductimétrique consiste à suivre l’évolution de la conductivité \(\sigma\) de la solution titrée au cours de l’ajout de la solution titrante.
On mesure la conductivité de la solution titrée pour chaque volume de solution titrante versée : on ajoute la solution titrante millilitre par millilitre avant et après l’équivalence.
La courbe de titrage est la courbe \(\sigma = f(V_{Sol.titrante versée})\) donnant les variations de la conductivité en fonction du volume de solution titrante versée.
Dans tous les cas, les deux droites de la courbe de titrage se coupent en un point (correspondant au changement de pente de la courbe) : ce point représente l'équivalence.
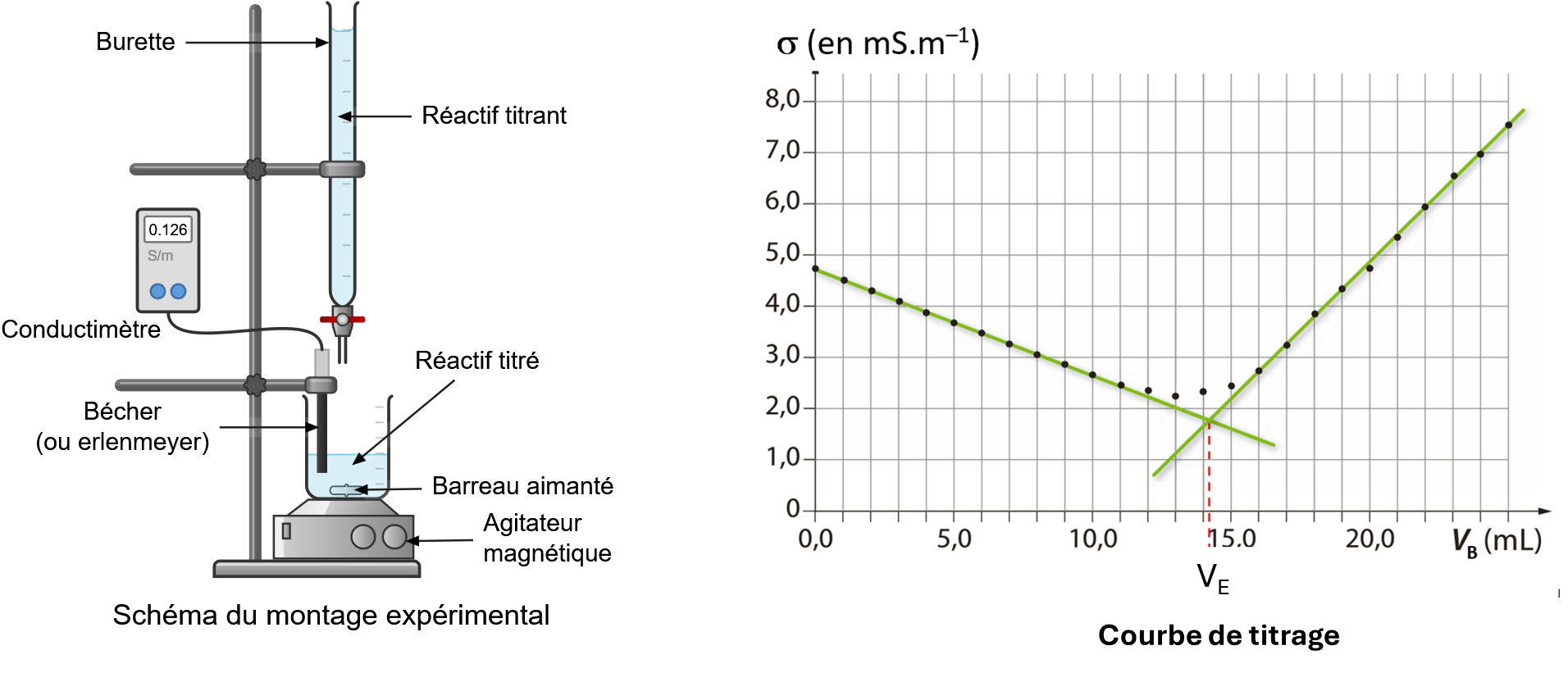
On lit alors son abscisse pour obtenir le volume équivalent VE.
b) 📉 Interpréter la courbe de titrage avec la loi de Kohlrausch⚓︎
Lorsqu'une solution ionique contient plusieurs espèces ioniques alors l'expression de la loi de Kohlrausch s'écrit de la façon suivante :
où :
- \(σ\) : conductivité en \(S.m^{-1}\)
- \(λ_i\) : conductivité molaire ionique de chaque espèce en \(S \cdot m^2 \cdot mol^{-1}\)
- \([X_i]\) : concentration de chaque espèce en \(mol \cdot L^{-1}\)
Dans ce cas, pour comprendre l'allure de la courbe de titrage conductimétrique il faut :
▪ Faire l'inventaire des ions présents dans le mélange réactionnel à chaque étape du titrage, y compris les ions spectateurs.
▪ Étudier les évolutions de leurs concentrations dans le mélange avant et après l'équivalence.
▪ Utiliser les conductivités molaires ioniques et la loi de Kohlrausch pour interpréter la variation de la conductivité
Exemple :⚓︎
On titre une solution de chlorure de sodium (\(Na^+_{(aq)}, Cl^-_{(aq)}\)) par une solution de nitrate d'argent (\(Ag^+{_{(aq)}}, NO_3^-{_{(aq)}}\)) avec un suivi conductimétrique.
On donnne ci-dessous la courbe de titrage et la conductivité des ions mis en jeu:
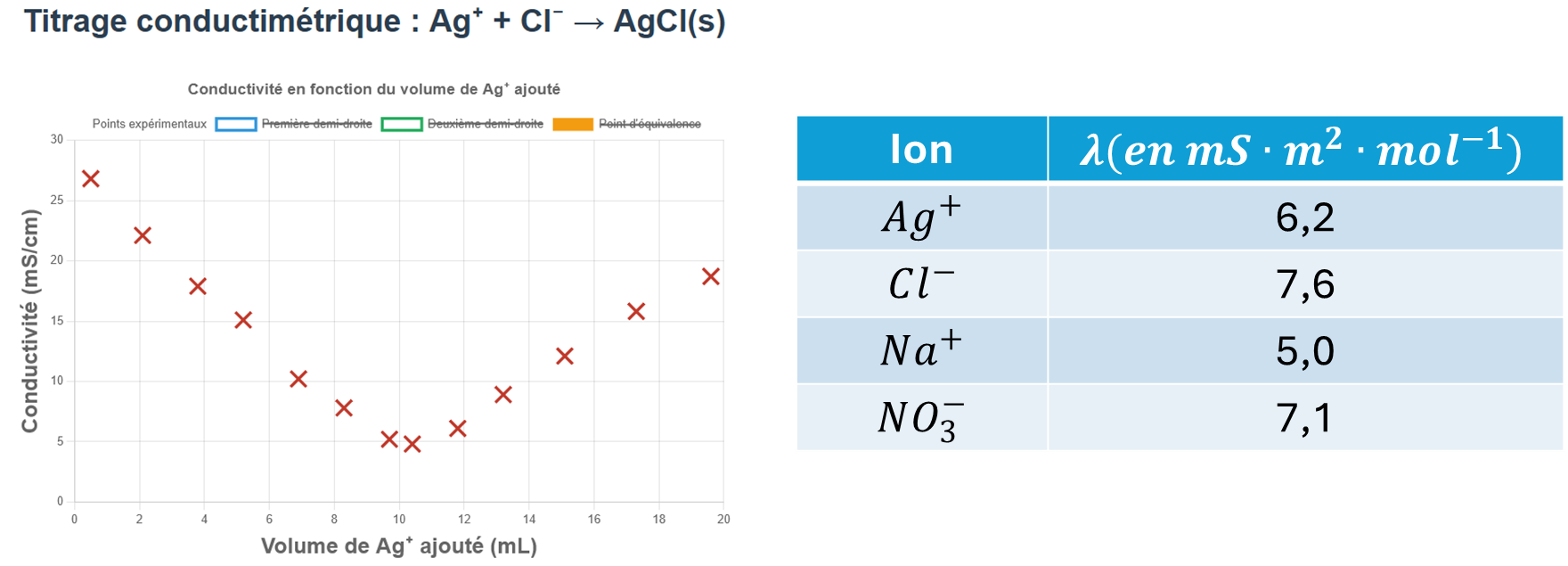
La réaction support du titrage est : \(Ag^+_{(aq)} + Cl^-_{(aq)} → AgCl_{(s)}\)
Les ions nitrate \(NO_3^-{_{(aq)}}\) et sodium \(Na^+_{(aq)}\) sont donc des ions spectateurs.
D'après la loi de Kohlrausch, la conductivité du mélange réactionnel s'écrit :
Évolution des quantités de matière
| Ions | Avant l'équivalence | Après l'équivalence |
|---|---|---|
| \(Ag^+\) | Espèce réagissante versée limitante \(n(Ag^+) = 0\) |
Espèce réagissante versée en excès \(n(Ag^+)\) ↗ quand \(V_{versé}\) ↗ |
| \(NO_3^-\) | Ion spectateur versé \(n(NO_3^-)\) ↗ quand \(V_{versé}\) ↗ |
Ion spectateur versé \(n(NO_3^-)\) ↗ quand \(V_{versé}\) ↗ |
| \(Na^+\) | Ion spectateur dans le bécher \(n(Na^+) = constante\) |
Ion spectateur dans le bécher \(n(Na^+) = constante\) |
| \(Cl^-\) | Espèce réagissante dans le bécher \(n(Cl^-)\) ↘ quand \(V_{versé}\) ↗ |
Espèce entièrement consommée \(n(Cl^-) = 0\) |
| Les ions \(NO_3^-\) moins conducteur remplacent les ions \(Cl^-\) qui disparaissent. La conductivité globale de la solution baisse et la courbe est une droite de pente négative | La quantité d'ions \(Ag^+\) et \(NO_3^-\) augmente dans le bécher. La conductivité globale de la solution augmente et la courbe est une droite de pente positive |
3. ▶️ Détermination de l'éqivalence⚓︎
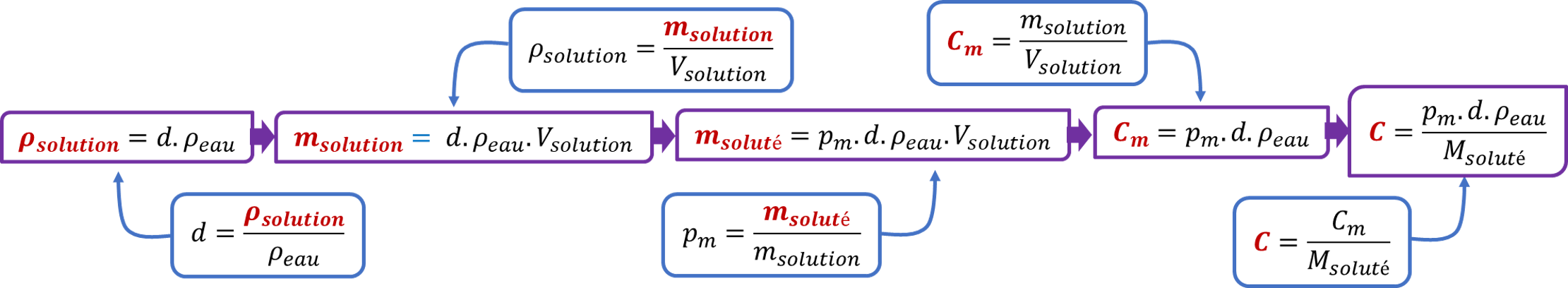
III. 🧾 Calcul de la concentration à partir du titre massique et de la densité⚓︎
A savoir
▶️ Capsule : Titre massique et densité
- Le pourcentage massique \(p_m\) (titre massique) d’une solution traduit sa teneur en soluté dissout, exprimé sans unité
- La densité \(d\) d’un liquide est le rapport entre sa masse volumique et celle de l’eau, exprimée sans unité :
➡️ On en déduit la concentration molaire d’une solution commerciale en fonction de \(d\) et \(p_m\).