Chapitre 7 : Évolution temporelle d’une transformation chimique⚓︎
▶️ Capsule : Le cours complet
▶️ Capsule : Le cours complet version 2
▶️ Capsule : Exercice de Bac
⏱️ I. Cinétique chimique⚓︎
🧠 A savoir
📚 1) Définition⚓︎
La cinétique chimique étudie l'évolution temporelle d'un système chimique au cours d'une transformation chimique.
Pour étudier une cinétique de réaction, il faut suivre l'évolution de la quantité ou de la concentration d'au moins un réactif ou un produit au cours du temps (l'équation de la réaction étant connue).
🔬 2) Méthodes de suivi⚓︎
On peut avoir recours à deux types de méthodes :
Méthode physique 📊 : on suit l'évolution d'une grandeur physique liée à la quantité ou la concentration (absorbance, conductivité, pH, ...).
Méthode chimique ⚗️ : on procède par exemple à des titrages successifs.
💡 Remarque : Pour suivre l'évolution temporelle d'une transformation chimique, le choix du capteur doit être adapté à la grandeur à mesurer, qui dépend de la quantité ou de la concentration de l'espèce chimique à suivre.
⏳ 3) Transformations lentes et rapides⚓︎
Transformation lente 🐌 : transformation dont on peut observer l'évolution sur une durée perceptible à l'œil nu ou à l'aide d'un appareil de mesure.
Transformation rapide ⚡ : transformation qui se produit en une durée trop courte pour que l'on puisse observer son évolution.
⚡ II. Modifier la vitesse d'une transformation chimique⚓︎
🧠 A savoir
🎯 1) Les facteurs cinétiques⚓︎
Définition 📖
Un facteur cinétique est un paramètre qui peut modifier la vitesse d'évolution d'une réaction chimique.
➡️ L'influence de la température 🌡️
- Température élevée : augmente l'agitation des particules et donc les chocs efficaces entre réactifs → la vitesse de réaction augmente
- Température faible : diminue l'agitation moléculaire → la vitesse de réaction diminue
💡 Application pratique : On conserve les aliments au réfrigérateur pour ralentir les réactions de dégradation.
▶️ Capsule : Influence de la température
➡️ L'influence de la concentration 🧪
À température constante, augmenter la concentration d'au moins un des réactifs augmente la vitesse de réaction (plus de particules réactives disponibles).
▶️ Capsule : Influence de la concentration
🔄 2) Les catalyseurs⚓︎
Définition 📖
Un catalyseur est une espèce chimique qui accélère une réaction sans modifier l'état final du système. Il est consommé puis régénéré au cours de la réaction.
Propriétés importantes ✨
- Le catalyseur ne figure pas dans l'équation de la réaction (car régénéré)
- Un catalyseur est spécifique d'une réaction donnée
- Lorsqu'une réaction utilise un catalyseur, on dit qu'elle est catalysée
Les trois types de catalyse 🎭 :
| Type de catalyse | Description |
|---|---|
| Catalyse homogène | Le catalyseur et les réactifs sont dans la même phase |
| Catalyse hétérogène | Le catalyseur et les réactifs sont dans des phases différentes |
| Catalyse enzymatique | Le catalyseur est une enzyme (catalyseur biologique) |
⚠️ Attention : Un catalyseur est une substance chimique, pas un facteur cinétique (contrairement à la température ou la concentration des réactifs).
▶️ Capsule : Catalyse enzymatique
📈 III. Suivi temporel de l'évolution d'un système⚓︎
🧠 A savoir
🔍 1) Méthodes de suivi cinétique⚓︎
Pour suivre l'évolution d'une réaction dans le temps, on mesure la concentration d'un réactif ou d'un produit à différents instants. Plusieurs méthodes existent :
- Spectrophotométrie 🌈 : mesure de l'absorbance d'une espèce colorée
- pH-métrie 🧪 : mesure du pH si la réaction produit ou consomme des ions H⁺
- Manométrie 📊 : mesure de la pression si la réaction produit un gaz
- Chromatographie 🧬 : séparation et identification des espèces chimiques
⚡ 2) Vitesse de réaction⚓︎
La vitesse d'une réaction se mesure par la variation de concentration d'une espèce chimique au cours du temps.
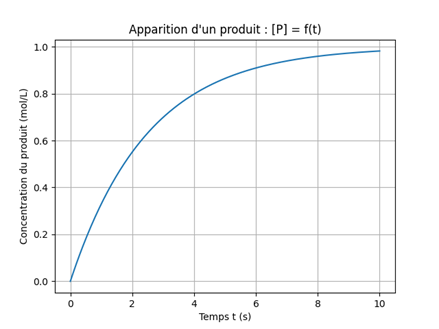
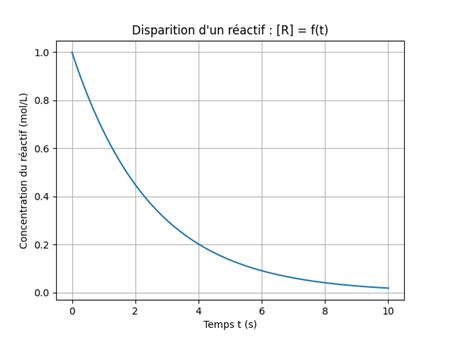
| 📈 Vitesse d'apparition d'un produit P | 📉 Vitesse de disparition d'un réactif R |
|---|---|
 |
 |
| Vitesse moyenne d'appariton entre tᵢ et tᵢ₊₁ \(v_{app}(P)=\frac{Δ[P]}{Δt}=\frac{[P]_{t_{i+1}}- [P]_{t_i}}{t_{i+1} - t_i}\) |
Vitesse de disparition moyenne entre tᵢ et tᵢ₊₁ \(v_{disp}(R)=-\frac{Δ[R]}{Δt}=-\frac{[R]_{t_{i+1}}- [R]_{t_i}}{t_{i+1} - t_i}\) |
| La vitesse instantanée est égale à la dérivée \(v_{app}(P)=\frac{d[P]}{dt}\) |
La vitesse instantanée est égale à la dérivée \(v_{disp}(R)=-\frac{d[R]}{dt}\) |
Méthode de détermination graphique 📐 :
1️⃣ Sur le graphique [R] = f(t), tracer la tangente à la courbe au point correspondant à l'instant t souhaité.
2️⃣ Choisir deux points A et B sur cette tangente, suffisamment éloignés l'un de l'autre pour améliorer la précision.
3️⃣ Relever les coordonnées de ces deux points
4️⃣ Calculer le coefficient directeur de la tangente : \(a = \frac{\Delta[R]}{\Delta t}\)
5️⃣ La vitesse de disparition est l'opposé de ce coefficient, la vitesse d'apparition est égale au coefficient.
▶️ Capsule : Calculer une vitesse de réaction
⏰ 3) Temps de demi-réaction⚓︎
Le temps de demi-réaction \(t_{1/2}\) est la durée nécessaire pour que la moitié du réactif limitant \(R_l\) soit consommée :
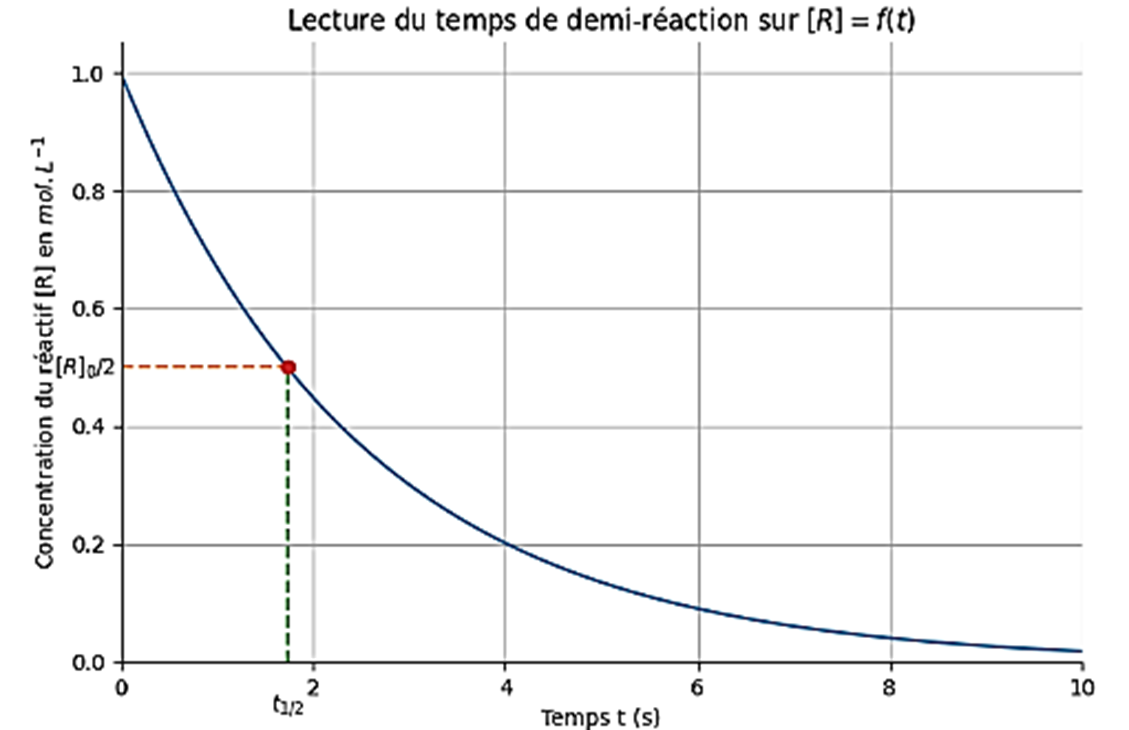
On peut aussi déterminer \(t_{1/2}\) à partir de l'évolution de la concentration d'un produit P au cours du temps :
▶️ Capsule : Temps de demi-réaction
📏 IV. Loi de vitesse d'ordre 1⚓︎
🧠 A savoir
▶️ Capsule : Loi de vitesse d'ordre 1
📖 1) Définition⚓︎
Une réaction suit une loi de vitesse d'ordre 1 par rapport au réactif limitant R si sa vitesse est proportionnelle à la concentration de R :
✅ 2) Méthodes de vérification⚓︎
Pour une réaction dans laquelle R est le réactif limitant, on peut vérifier que la réaction est d'ordre 1 par rapport à R par trois méthodes :
Méthode 1 : Vérification du temps de demi-réaction ⏱️
Le temps de demi-réaction est indépendant de la concentration initiale [R]₀.
Si on réalise plusieurs expériences avec des concentrations initiales différentes et que \(t_{1/2}\) reste constant, alors la réaction est d'ordre 1.
Méthode 2 : Vérification de la proportionnalité 📊
Les vitesses d'apparition des produits et de disparition des réactifs sont proportionnelles à la concentration [R] du réactif limitant au cours du temps : \(v = k \times [R]\)
📊 Graphiquement : La courbe \(v = f([R])\) est une droite qui passe par l'origine. Le coefficient directeur de cette droite est la constante de vitesse k.
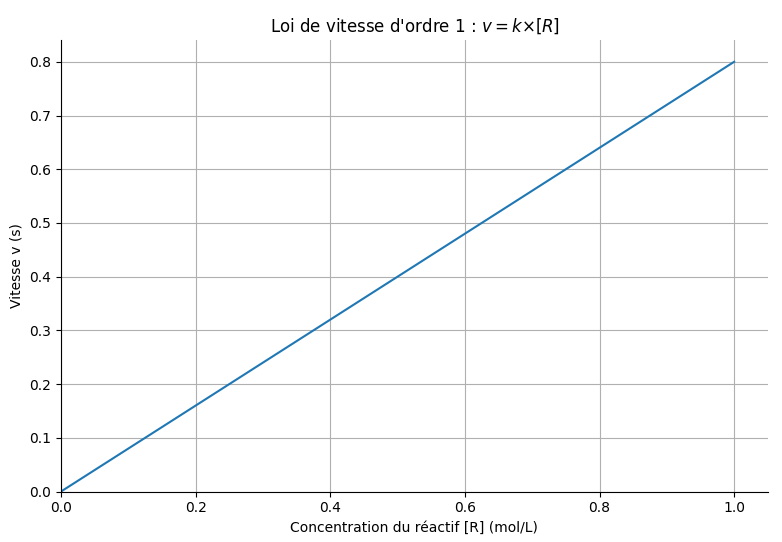
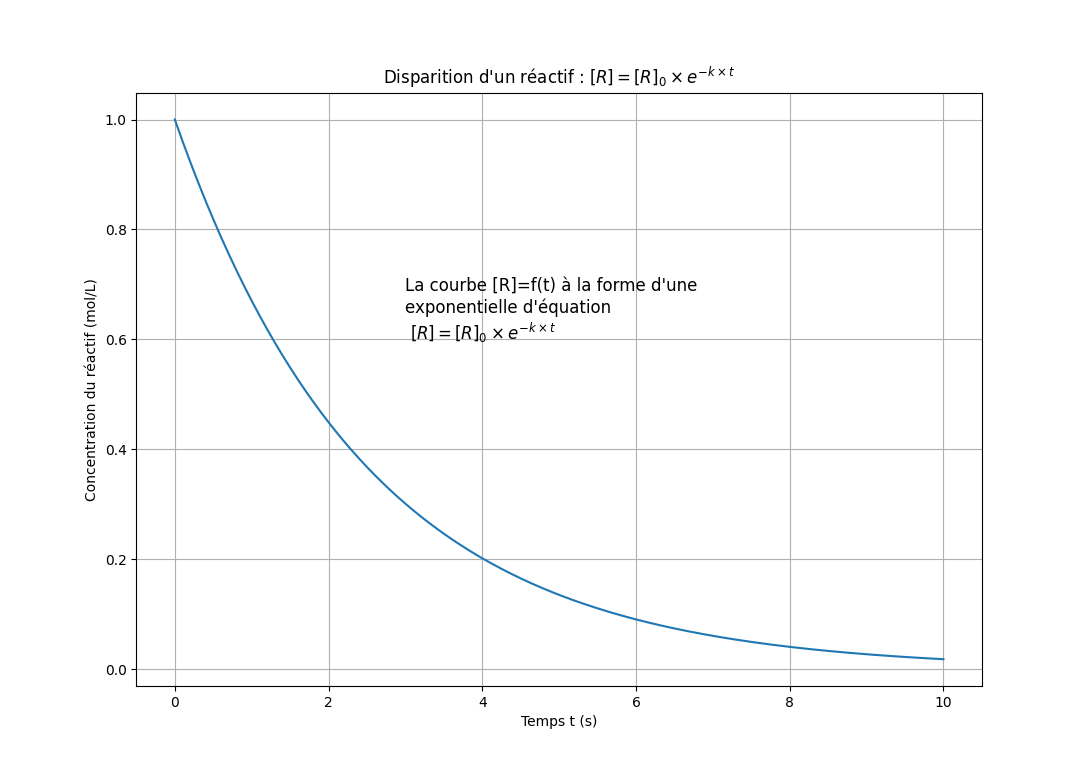
Méthode 3 : Vérification de la loi exponentielle 📉
La concentration obéit à une loi exponentielle décroissante :
où k est la constante de vitesse.
📊 Graphiquement : La courbe [R] = f(t) a une allure exponentielle
🔗 3) Relation entre k et t₁/₂⚓︎
Pour une réaction d'ordre 1, le temps de demi-réaction et la constante de vitesse sont liés par la relation :
Cette relation montre que plus k est grand, plus \(t_{1/2}\) est petit, donc plus la réaction est rapide.