Chapitre 10 : Transformations spontanées dans les piles⚓︎
▶️ Capsule : Qu'est-ce qu'une pile
▶️ Capsule : Fiche de révision - les piles
🔋 I. La pile, siège de transformations spontanées⚓︎
🧠 A savoir
🔌 1) Constitution d'une pile⚓︎
Le principe d'une pile est de convertir l'énergie chimique 🧪 en énergie électrique ⚡ à partir d'une réaction d'oxydoréduction spontanée.
Une pile est constituée de 2 compartiments distincts, appelés « demi-piles » :
- Chaque demi-pile est constituée d'un couple Ox/Red de type Mⁿ⁺(aq)/M(s) en général : M est un métal (l'électrode) et Mⁿ⁺ est un ion en solution dans « l'électrolyte ».
- Les deux demi-piles sont reliées par un « pont salin » qui permet de fermer le circuit et d'assurer la neutralité des solutions.
La tension positive U₀ mesurée entre les deux électrodes à vide, quand la pile ne débite pas donc, est la tension à vide. La borne V du voltmètre ou la borne A de l'ampèremètre définit la borne positive de la pile.
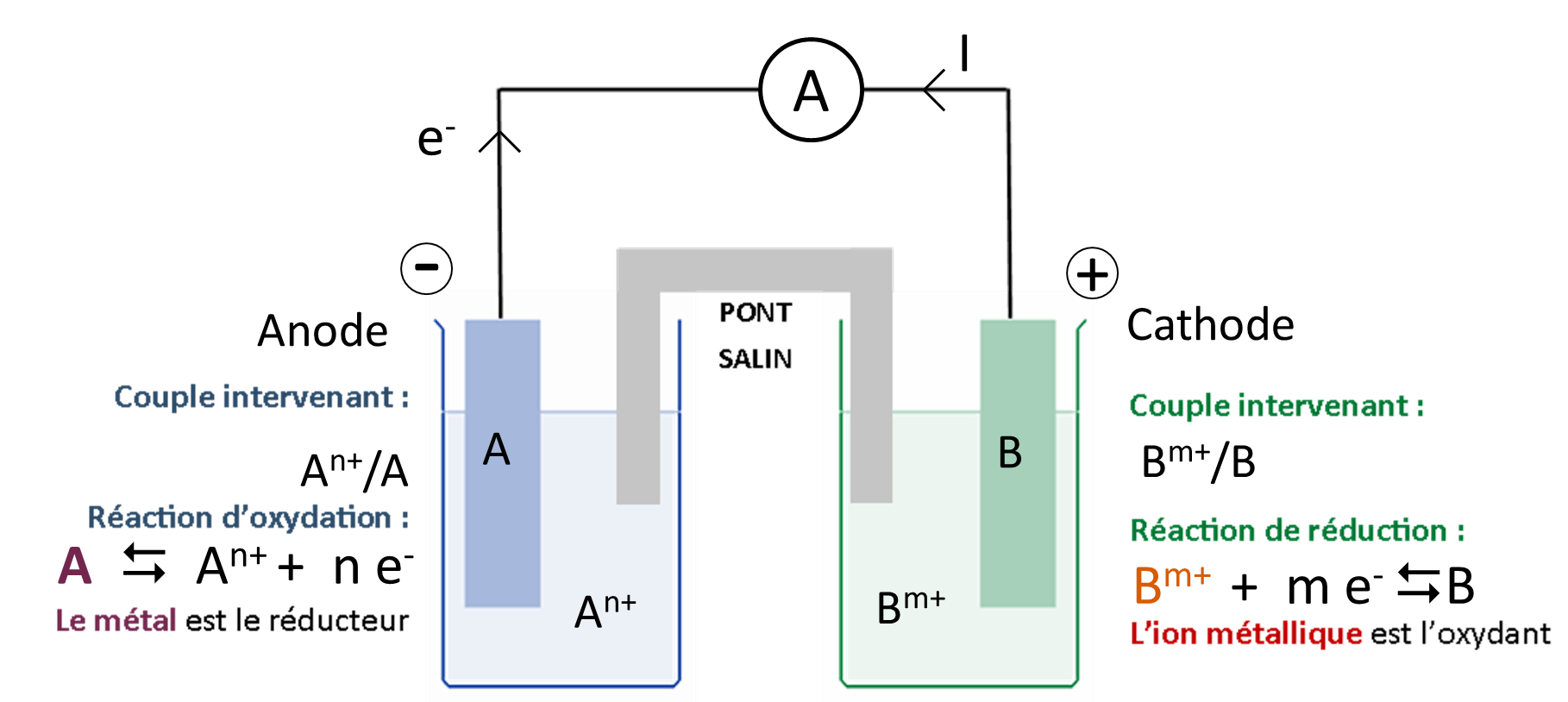
🔁 2) Fonctionnement d'une pile⚓︎
Lorsqu'on relie les deux électrodes par un fil conducteur 🔌, du courant électrique circule, ce qui prouve que les réactions se produisent dans les demi-piles, et des électrons sont transférés du réducteur vers l'oxydant.
Lors du fonctionnement d'une pile, des électrons circulent dans le fil conducteur (circuit extérieur) et des ions circulent dans le pont salin et les solutions pour assurer la neutralité électrique des solutions.
À la borne négative (anode) ⊖ : il y a une oxydation : les électrons sont libérés par le réducteur et vont circuler dans le circuit extérieur.
À la borne positive (cathode) ⊕ : il y a une réduction : les électrons sont captés par l'oxydant après avoir circulé dans le circuit extérieur.
L'équation de la réaction de fonctionnement de la pile est établie en combinant les deux réactions qui ont lieu aux électrodes.
💡 Rappel : Le courant électrique circule de la borne positive à la borne négative dans le circuit extérieur (« sens conventionnel ») alors que les électrons vont dans le sens inverse.
▶️ Capsule : Rappels sur l'oxydoréduction
▶️ Capsule : Anode ou cathode ?
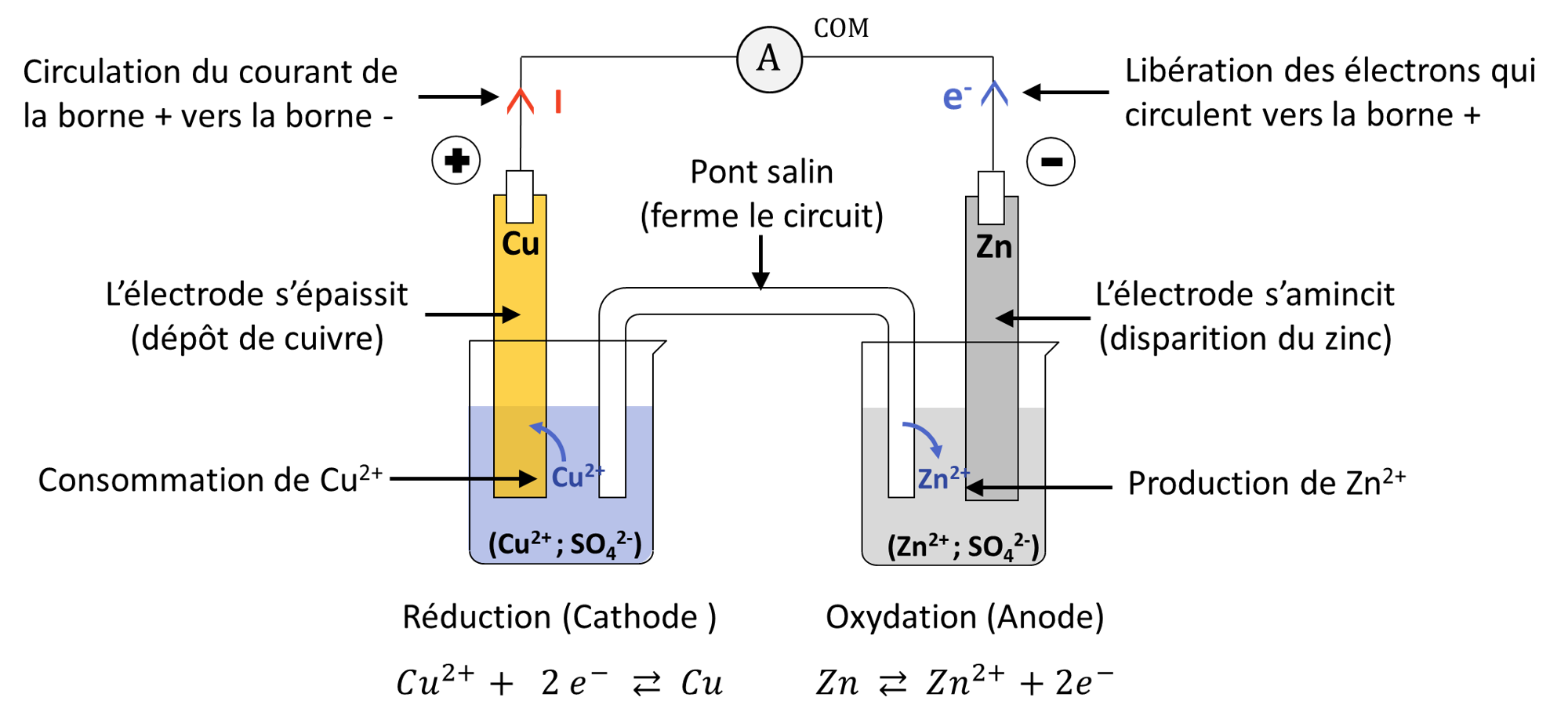
🔬 3) Exemple : la pile Daniell (celle réalisée en TP)⚓︎
Le schéma ci-dessous dédrit le fonctionnement de la pile cuivre-zinc (ou pille Daniell) donc l'équation de fonctionnement est :
⏳ II. Usure d'une pile⚓︎
🧠 A savoir
⚖️ 1) Évolution vers l'équilibre⚓︎
Lorsqu'on relie les deux électrodes par un fil conducteur, du courant électrique circule, le système chimique évolue, il est hors équilibre : Qr ≠ K
La réaction chimique de la pile possède une constante d'équilibre K vers laquelle tend le quotient de réaction au fur et à mesure que la pile débite : il y a usure de la pile et lorsque Qr = K, l'équilibre chimique est atteint et la pile ne fonctionne plus ; elle est « usée ».
📦 2) Capacité d'une pile⚓︎
Pour adapter la pile à l'usage souhaité, il convient d'évaluer sa capacité électrique, notée Q.
La capacité électrique d'une pile est la charge électrique maximale qu'elle peut débiter durant sa durée de vie :
ℹ️ Remarques :
- Le produit \(F = \mathcal{N}_A \times e\) est aussi appelé constante de Faraday avec F = 96500 C·mol⁻¹
- La quantité de matière d'électrons échangés se détermine à partir de la quantité du réactif limitant.
- La capacité est souvent indiquée sur les piles du commerce dans une autre unité : l'ampère-heure (Ah)
De plus, en supposant que la pile débite un courant d'intensité constante I pendant une durée Δt, alors :
▶️ Capsule : Capacité d'une pile
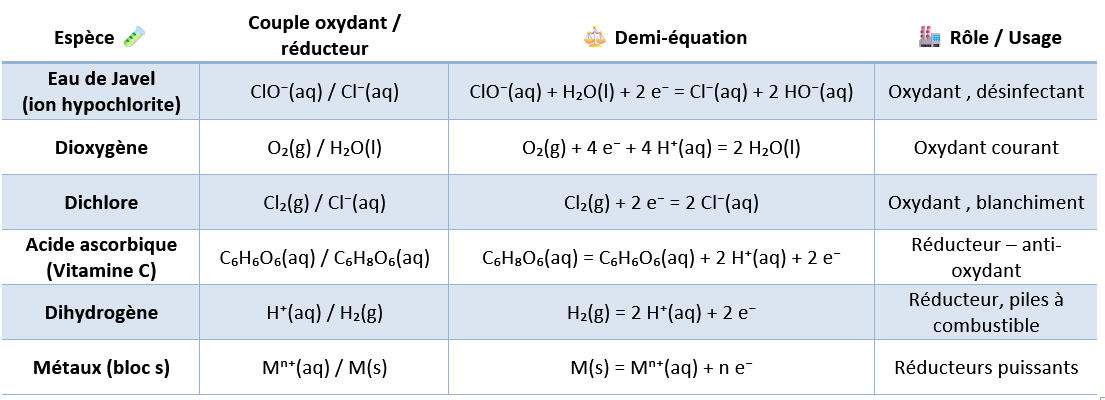
🧪 III. Couples oxydant-réducteur usuels⚓︎
🧠 A savoir
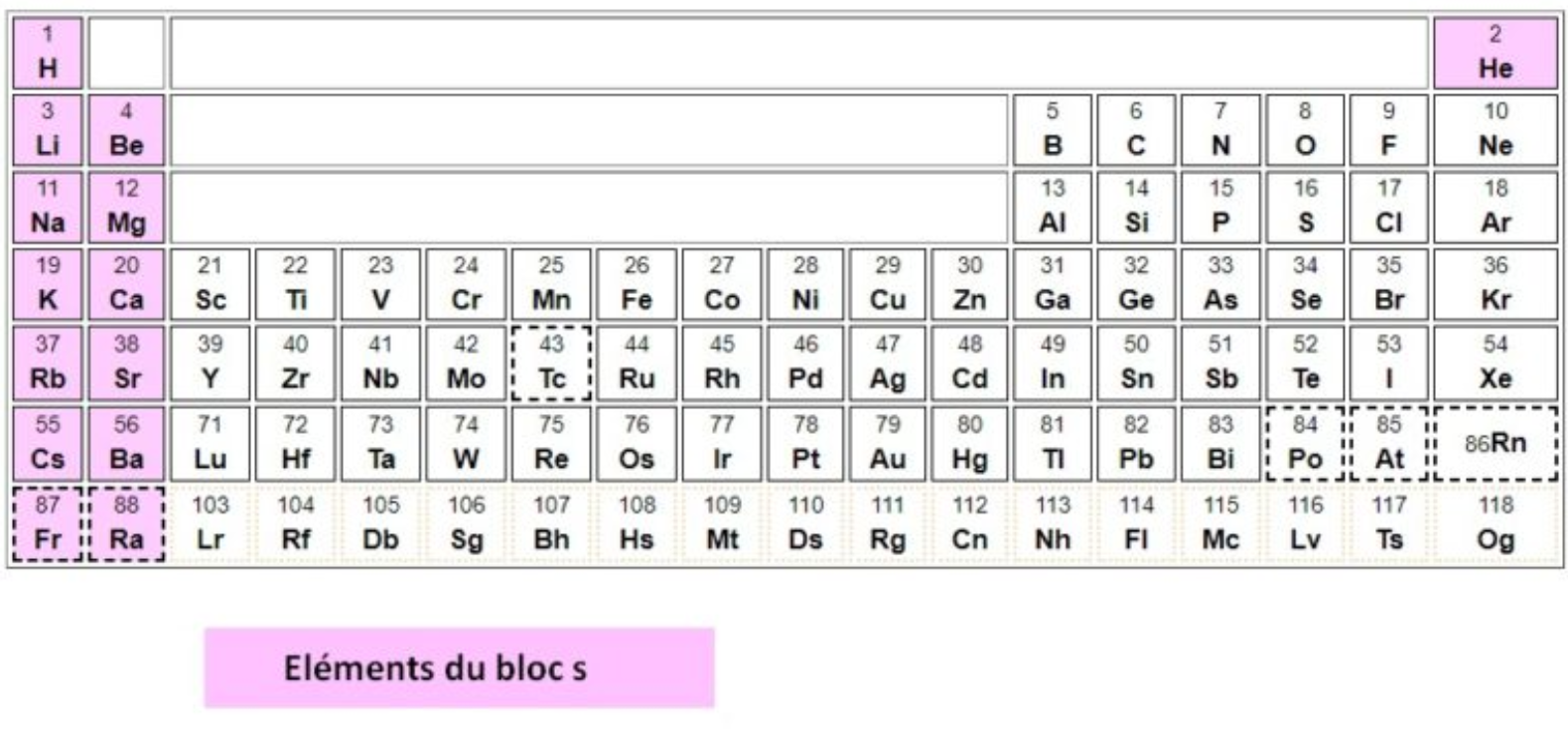
⚛️ 1) Métaux du bloc s⚓︎
Pour optimiser les piles, on peut utiliser les métaux dont les éléments appartiennent aux colonnes 1 et 2 (bloc s) de la classification périodique car ils sont très réducteurs (ils perdent facilement le seul électron de valence ou les 2 électrons de valence qu'ils possèdent ⚛️).
Il s'agit de la famille des alcalins et alcalino-terreux.
📋 2) Autres couples usuels⚓︎
▶️ Capsule : Couples redox usuels