Chapitre 12 : Force des acides et des bases⚓︎
▶️ Capsule : Le cours complet
▶️ Capsule : Le cours complet 2
💧 I. Le produit ionique de l'eau⚓︎
🧠 A savoir
L'eau est un ampholyte : il se produit une réaction entre l'acide \(\ce{H2O_{(\ell)}}\) (du couple \(\ce{H2O_{(\ell)}/HO^-_{(aq)}}\)) et la base \(\ce{H2O_{(\ell)}}\) (du couple \(\ce{H3O^+_{(aq)}/H2O_{(\ell)}}\)).
Cette transformation est appelée « autoprotolyse de l'eau » et est modélisée par l'équation de réaction suivante :
Cette réaction explique la formation des ions oxonium et hydroxyde dans l'eau pure.
L'état d'équilibre de la réaction d'autoprotolyse de l'eau est associé à une constante d'équilibre notée Ke, appelée ici produit ionique de l'eau défini par la relation :
Le pKe de l'eau est une grandeur, sans dimension, qui dépend de la température et définie par :
À 25°C, quelle que soit les concentrations des ions oxonium et hydroxyde, on aura toujours \(K_e = 1{,}0 \times 10^{-14}\) soit \(pK_e = 14{,}0\).
▶️ Capsule : Produit ionique de l'eau
⚗️ II. Réaction d'un acide ou d'une base avec l'eau⚓︎
🧠 A savoir
🧪 1) Réaction d'un acide avec l'eau⚓︎
Soit une espèce acide AH que l'on introduit dans l'eau et dont la concentration apportée en soluté apporté est C.
| Acide Fort 💪 | Acide Faible 🤏 | |
|---|---|---|
| Couples mis en jeu | AH/A⁻ et H₃O⁺/H₂O | AH/A⁻ et H₃O⁺/H₂O |
| Réaction | \(\ce{AH + H2O -> A- + H3O+}\) | \(\ce{AH + H2O <=> A- + H3O+}\) |
| Concentrations finales en H₃O⁺ | \([\ce{H3O+}]_f = C\) | \([\ce{H3O+}]_f < C\) |
| Calcul du pH | \(pH = -\log\left(\frac{C}{C^0}\right)\) | \(pH > -\log\left(\frac{C}{C^0}\right)\) |
| Taux d'avancement final | \(\tau = 1\) | \(\tau < 1\) |
| Nature de la transformation | Transformation est totale | Transformation non totale : les espèces AH, A⁻ et H₃O⁺ coexistent dans la solution. |
Exemples 📝 :
-
Le chlorure d'hydrogène HCl est un acide fort : HCl n'existe donc pas en solution aqueuse et la solution obtenue est une solution d'acide chlorhydrique contenant les ions oxonium et chlorure, notée (H₃O⁺₍aq₎ ; Cl⁻₍aq₎)
-
L'acide éthanoïque CH₃COOH est un acide faible : \(\ce{CH3COOH_{(aq)} + H2O_{(\ell)} <=> CH3COO^-_{(aq)} + H3O^+_{(aq)}}\) en solution, \(\ce{CH3COOH_{(aq)}}\) coexiste avec \(\ce{CH3COO^-_{(aq)}}\) et \(\ce{H3O^+_{(aq)}}\)
🧫 2) Réaction d'une base avec l'eau⚓︎
Soit une espèce basique B que l'on introduit dans l'eau et dont la concentration apportée en soluté apporté est C.
| Base Forte 💪 | Base Faible 🤏 | |
|---|---|---|
| Couples mis en jeu | B/BH⁺ et H₂O/HO⁻ | B/BH⁺ et H₂O/HO⁻ |
| Réaction | \(\ce{B + H2O -> BH+ + HO-}\) | \(\ce{B + H2O <=> BH+ + HO-}\) |
| Concentrations finales en HO⁻ | \([\ce{HO-}]_f = C\) | \([\ce{H3O+}]_f < C\) |
| Calcul du pH | \(pH = pK_e + \log\left(\frac{C}{C^0}\right)\) | \(pH < pK_e + \log\left(\frac{C}{C^0}\right)\) |
| Taux d'avancement final | \(\tau = 1\) | \(\tau < 1\) |
| Nature de la transformation | Transformation totale | Transformation non totale : les espèces B, BH⁺ et HO⁻ coexistent dans la solution. |
Exemples 📝 :
-
L'hydroxyde de sodium NaOH est une base forte : NaOH n'existe donc pas en solution aqueuse et la solution obtenue est une solution d'hydroxyde de sodium (ou soude) contenant les ions hydroxyde et sodium, notée (Na⁺₍aq₎ ; HO⁻₍aq₎)
-
L'ammoniac NH₃ est une base faible : \(\ce{NH3_{(g)} + H2O_{(\ell)} <=> NH4^+_{(aq)} + HO^-_{(aq)}}\) en solution, NH₃ coexiste avec NH₄⁺ et HO⁻.
📊 III. Constante d'acidité d'un couple acide-base⚓︎
🧠 A savoir
Il existe des réactions acide-base non totales : Il est donc possible d'associer une constante d'équilibre pour ces transformations. On considère la réaction entre l'acide d'un couple AH/A⁻ et l'eau en tant que base dans le couple H₃O⁺/H₂O. L'équation de cette réaction est modélisée par : \(\ce{AH + H2O <=> A- + H3O+}\)
La constante d'acidité Ka est la constante d'équilibre associée à l'équation de la réaction d'un acide faible AH avec l'eau. Elle est définie par la relation :
- \([\ce{H3O+}]_{eq}\), \([\ce{A-}]_{eq}\), \([\ce{AH}]_{eq}\) sont les concentrations des espèces à l'équilibre
- \(K_a\) est la constante d'acidité du couple AH/A⁻ (donc sans unité)
- \(C^0 = 1\text{ mol·L}^{-1}\) est la concentration standard.
- L'eau, solvant, n'intervient pas dans l'expression de Ka
Le pKa d'un couple acide/base est une grandeur, sans dimension, comprise entre 0 et 14 et caractéristique du couple défini par :
Les valeurs de Ka et pKa sont connues et répertoriées dans des tables à une température donnée (généralement 25°C).
▶️ Capsule : Constante d'acidité Ka et pKa
▶️ Capsule : Constante d'acidité et taux d'avancement
⚖️ IV. Forces comparées des acides et des bases dans l'eau⚓︎
🧠 A savoir
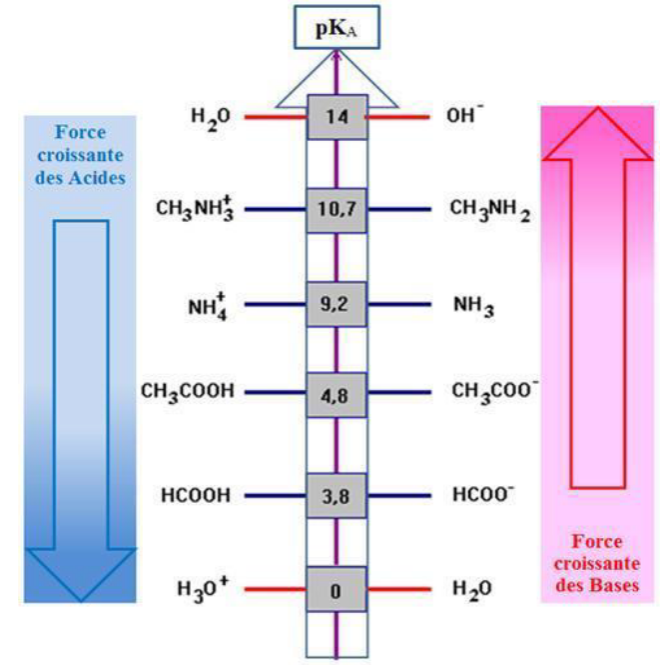
La force d'un acide ou d'une base correspond à sa capacité à réagir avec l'eau : la valeur de \(K_a\) (ou de \(pK_a\)) permet de caractériser la force d'un acide.
-
🔴 Un acide réagissant avec l'eau est d'autant plus fort que sa constante d'acidité \(K_a\) est grande (et donc son \(pK_a\) petit).
-
🔵 Une base réagissant avec l'eau est d'autant plus forte que sa constante d'acidité \(K_a\) est faible (et donc son \(pK_a\) est grand).
Remarques 💡 :
-
L'acide le plus fort dans l'eau est l'ion oxonium H₃O⁺ ; la base la plus forte dans l'eau est l'ion hydroxyde HO⁻
-
Les pKa des couples acide-base sont compris entre ceux des deux couples de l'eau.
▶️ Capsule : Acide FORT ou acide FAIBLE ?
▶️ Capsule : Force des ACIDES et Échelle de pKa
▶️ Capsule : Force d'un acide exo du bac
📈 V. Espèce prédominante d'un couple⚓︎
🧠 A savoir
Soit un couple acide faible/base faible présent dans une solution aqueuse dont on connait le pH. Les deux espèces chimiques (AH et A⁻) sont présentes simultanément dans la solution.
Le pH d'une solution contenant un acide faible AH et sa base conjuguée A⁻ est lié au Ka du couple par la relation :
(équation de Henderson-Hasselbalch)
Démonstration 🔍 :
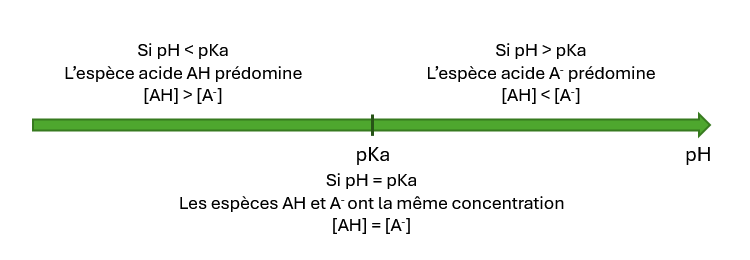
Le diagramme de prédominance d'un couple acide faible/base faible est un axe gradué de pH sur lequel apparaissent la valeur du pKa du couple et les domaines où les espèces conjuguées prédominent :
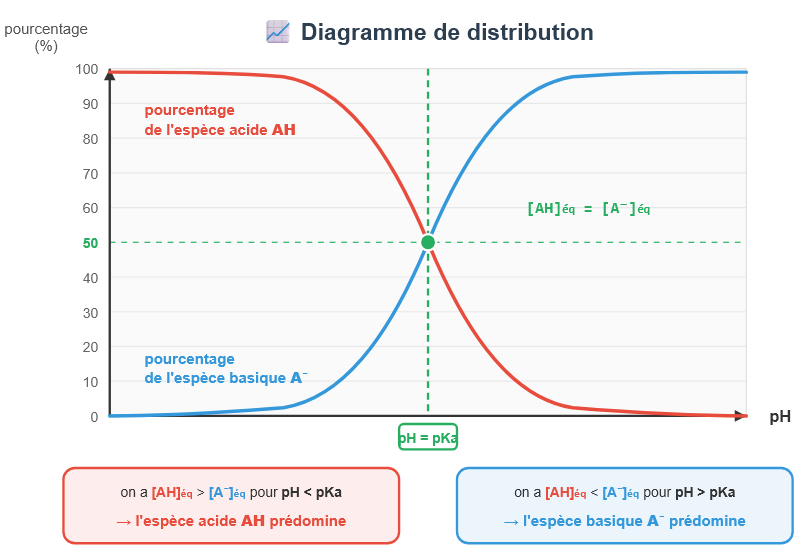
Le diagramme de distribution représente les pourcentages d'un acide et de sa base conjuguée en fonction de la valeur du pH de la solution ; il permet de connaître la composition de la solution.
▶️ Capsule : Diagramme de prédominance
🔬 VI. Applications⚓︎
🧠 A savoir
🧬 1) Les acides α-aminés⚓︎
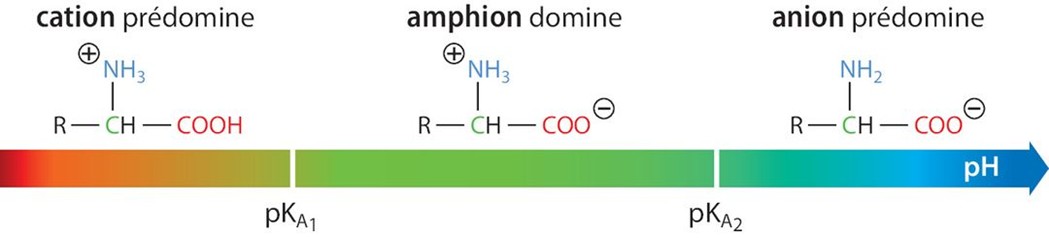
Les acides α-aminés possèdent deux groupes caractéristiques possédant des propriétés acido-basiques caractérisés par deux valeurs du pKa :
- Un groupe carboxyle membre du couple R-COOH/R-COO⁻ de pKa₁.
- Un groupe amino membre du couple R-NH₃⁺/R-NH₂ de pKa₂.
Le diagramme de prédominance se présente alors ainsi :
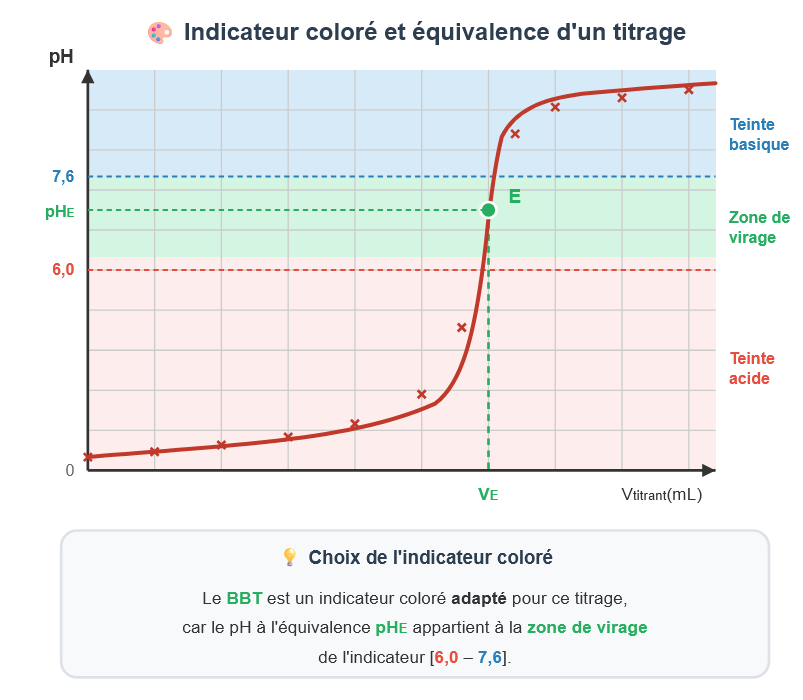
🎨 2) Indicateur coloré et équivalence d'un titrage⚓︎
Un indicateur coloré est une solution contenant un couple acido-basique dont les espèces conjuguées n'ont pas la même couleur. Sa zone de virage correspond à l'intervalle de pH dans lequel il passe d'une teinte à l'autre (teinte sensible).
💡 Un indicateur coloré peut ainsi être utilisé lors d'un titrage pour déterminer l'équivalence si le pH à l'équivalence se situe dans sa zone de virage.
🧴 3) Solution tampon et contrôle du pH⚓︎
Une solution tampon est une solution dont le pH varie peu par ajout d'une petite quantité d'acide ou de base, et par dilution modérée.
Elle est constituée d'un acide faible et sa base conjuguée en concentrations de même ordre de grandeur. Son pH est proche du pKa du couple.
Dans les milieux biologiques, les processus biochimiques sont très sensibles aux variations de pH, et la majorité des enzymes ne sont actives que pour un pH proche de 7 : le pH du sang est ainsi maintenu proche de 7,4 grâce à la présence de plusieurs couples acido-basiques, dissous dans le plasma sanguin, qui exercent un effet tampon.
🩸 On peut par exemple citer le couple (CO₂,H₂O)/HCO₃⁻ dont le pKa vaut 6,3 à 37°C.