Chapitre 11 : Transformation forcée d'un système⚓︎
▶️ Capsule : Le cours complet
▶️ Capsule : L'électrolyse
⚡ I. Transformation forcée d'un système⚓︎
🧠 A savoir
📖 1) Définitions⚓︎
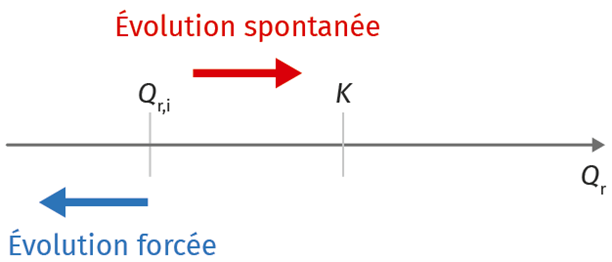
Une réaction d'oxydo-réduction peut se dérouler spontanément dans un sens bien déterminé entre l'oxydant d'un couple et le réducteur d'un autre couple. Cette réaction évolue vers un état d'équilibre défini par sa constante d'équilibre K(T). On parle de transformation spontanée.
Il est possible de forcer la réaction à se dérouler dans le sens contraire grâce à un générateur : les échanges d'électrons se font dans le sens contraire et le système va alors convertir de l'énergie électrique en énergie chimique. On parle de transformation forcée.
🔬 2) Exemple : réaction entre les couples I₂(aq) / I⁻(aq) et Zn²⁺(aq) / Zn(s)⚓︎
Réaction spontanée ⚡ :
Réaction forcée 🔌 :
qui implique les réactions (forcée) aux électrodes :
- \(\ce{2 I-(aq) -> I2(aq) + 2 e-}\) (Oxydation)
- \(\ce{Zn^{2+}(aq) + 2 e- -> Zn(s)}\) (Réduction)
🔋 II. Réaction forcée par électrolyse⚓︎
🧠 A savoir
⚗️ 1) L'électrolyseur⚓︎
L'électrolyseur permet de réaliser une transformation forcée, appelée une électrolyse : il s'agit d'un récepteur électrique constitué de deux électrodes plongeant dans une solution appelée électrolyte et reliées à un générateur, qui impose le sens de circulation des électrons.
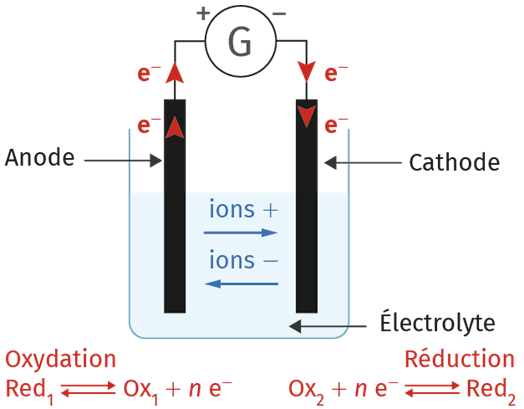
La borne négative ⊖ du générateur est reliée à l'électrode de l'électrolyseur sur laquelle a toujours lieu la réduction de l'oxydant. Cette électrode est la cathode.
La borne positive ⊕ du générateur est reliée à l'électrode de l'électrolyseur sur laquelle a toujours lieu l'oxydation du réducteur. Cette électrode est l'anode.
🔌 2) Conversion d'énergie dans l'électrolyseur⚓︎
Un électrolyseur convertit de l'énergie électrique en énergie chimique, en utilisant les électrons fournis par le générateur de courant continu.
La quantité d'électricité Q débitée par le générateur délivrant un courant d'intensité I à l'électrolyseur, pendant une durée \(\Delta t\) est :
La quantité d’électricité Q stockée dans la ile dépend également de la quantité d’électrons échangés \(n(e^-)\):
💧 3) Application : électrolyse de l'eau⚓︎
L'électrolyse de l'eau peut être effectuée à l'aide d'une cuve à électrolyse dans laquelle on a versé de l'acide sulfurique selon le dispositif expérimental ci-dessous :
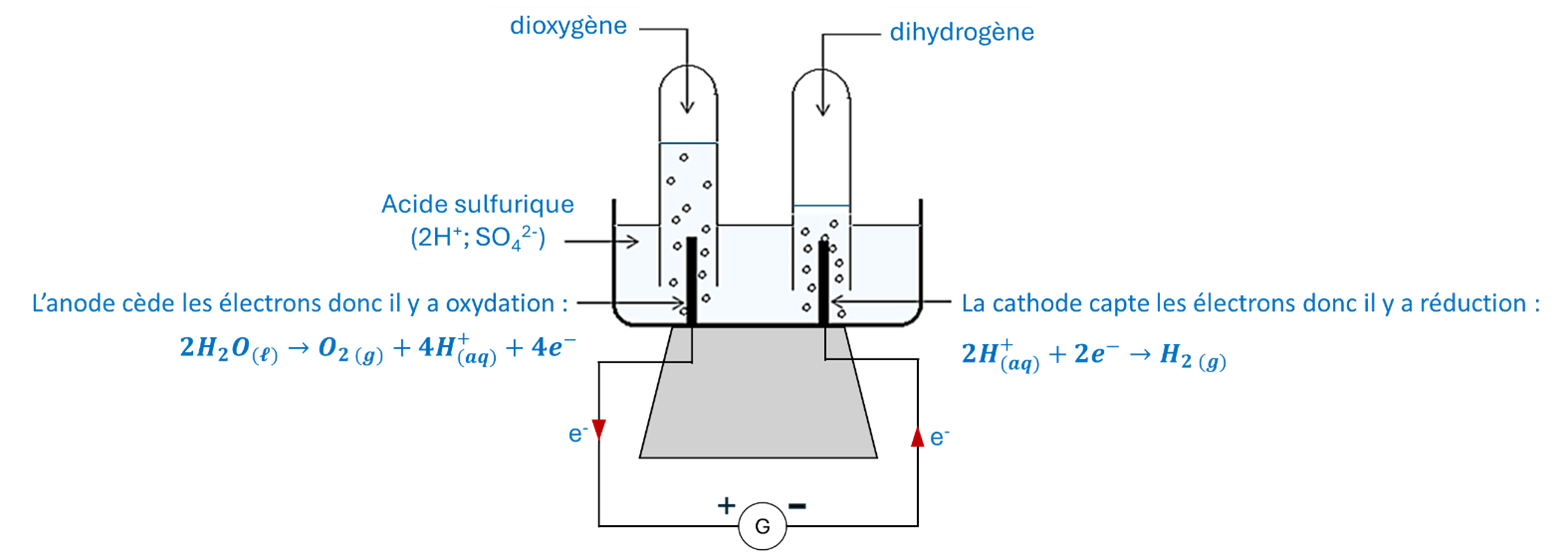
L'équation de la C qui décrit le fonctionnement global de l'électrolyseur est la somme des demi-équations aux électrodes :
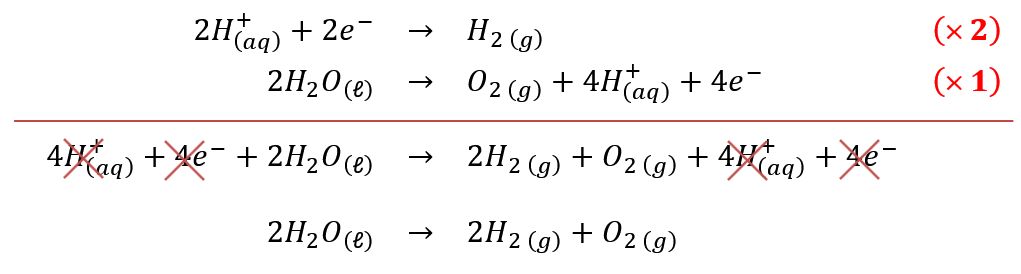
L'équation de la réaction globale de fonctionnement de l'électrolyseur est :
La quantité de matière de dihydrogène formé est égale au double de la quantité de matière de dioxygène formé donc le volume de gaz dihydrogène formé est approximativement égal au double du volume de gaz dioxygène formé.
🔄 III. Stockage et conversion d'énergie chimique⚓︎
🧠 A savoir
ℹ️ Remarque : Les exemples sont à connaître mais pas les réactions chimiques qui ne sont là que pour illustrer ces exemples.
🔋 1) Conversion d'énergie dans une pile⚓︎
Un convertisseur assure la conversion d'une forme d'énergie en une ou plusieurs autres formes :
Lorsqu'elle débite du courant électrique, une pile convertit l'énergie chimique en énergie électrique grâce à une réaction spontanée d'oxydoréduction. Les réactions en jeu sont irréversibles, on ne peut pas forcer la transformation dans l'autre sens.

🔁 2) Conversion d'énergie dans un accumulateur⚓︎
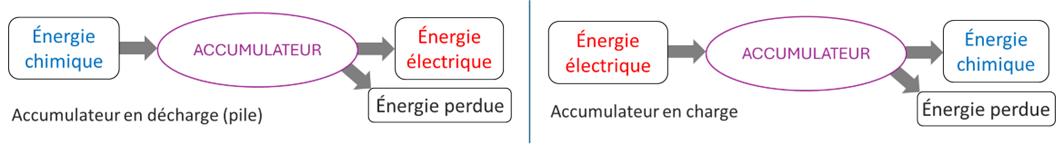
Les accumulateurs sont des systèmes électrochimiques rechargeables : lors de la décharge, une transformation spontanée d'oxydoréduction a lieu et lors de la charge, la transformation inverse forcée est réalisée.
Exemple : La batterie au plomb 🔋
Elle se caractérise essentiellement par :
- La tension nominale U qui dépend du nombre d'éléments ;
- La capacité de stockage, notée Q : quantité d'énergie disponible. Elle s'exprime en ampère-heure ;
- Le courant maximal qu'elle peut fournir pendant quelques instants, ou courant de crête.
Les réactions électrochimiques aux électrodes (lors de la décharge) sont les suivantes :
- Anode (oxydation) : \(\ce{Pb(s) + SO4^{2-}(aq) -> PbSO4(s) + 2 e-}\)
- Cathode (réduction) : \(\ce{PbO2(s) + 4 H+(aq) + SO4^{2-}(aq) + 2 e- -> PbSO4(s) + 2 H2O(l)}\)
💡 Remarque : Une batterie est un ensemble d'accumulateurs raccordés en série, afin d'obtenir la tension désirée et réunis dans un même boîtier.
🌿 3) Les organismes chlorophylliens⚓︎
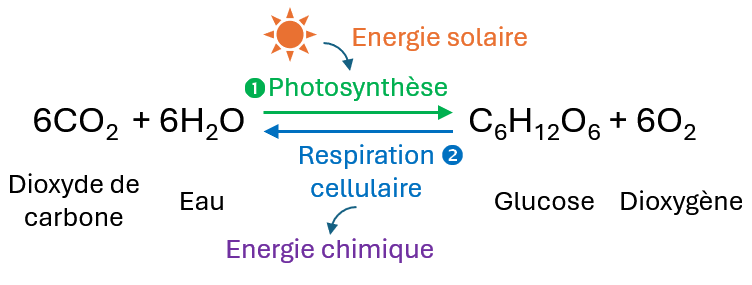
La photosynthèse est le processus bioénergétique qui permet à ces organismes de synthétiser de la matière organique en utilisant l'énergie lumineuse, l'eau et le dioxyde de carbone.
1️⃣ Durant la journée ☀️ ces organismes convertissent de l’énergie transportée par la lumière du Soleil sous forme d’énergie chimique (glucose) : c’est la photosynthèse qui est une transformation forcée.
2️⃣ Durant la nuit 🌙 ces organismes récupèrent de l’énergie chimique en oxydant la molécule de glucose : c’est la réaction inverse de la photosynthèse appelée respiration cellulaire qui est une réaction spontanée.
▶️ Capsule : Exercice du bac
▶️ Capsule : QCM pour s'entrainer